Diagnose
30. August 2017
Erythema-anulare-centrifugum-artige Psoriasis cum pustulatione
Diskussion
Die Erythema-anulare-centrifugum-artige Psoriasis cum pustulatione (EACP) ist eine Sonderform der Psoriasis pustulosa generalisata (Typ von Zumbusch) mit einem milderen Verlauf und fehlenden Allgemeinsymptomen [1]. Das Krankheitsbild wurde bereits 1933 von Milian und Katchoura als „Psoriasis pustulosa benigna“ beschrieben [2], als Erstbeschreiber gilt jedoch Lapière [3]. Für das Krankheitsbild charakteristisch ist das gyrierte, circinäre oder anuläre Anordnungsmuster, welches gekennzeichnet wird durch die rasche zentrifugale Ausbreitung sowie durch den trizonalen Aufbau der Einzelläsionen; (i) ein zentrales livides Erythem, (ii) eine Übergangszone mit colleretteartiger (halskrausenartiger) Schuppung, (iii) ein „aktiver“ peripherer Anteil mit multiplen, dicht stehenden, beetartig angeordneten, nicht follikulär gebundenen, stecknadelkopfgroßen Pusteln auf hellrotem Grund (Abbildung 1) [4]. Die Aktivierung und Rekrutierung neutrophiler Granulozyten mit konsekutiver Pustelbildung wird unter anderem durch die Zytokine IL-8 (Interleukin-8), GM-CSF (granulocyte macrophage colony-stimulating factor) und MCP (monocyte chemoattractant protein) vermittelt [5, 6].
Die Prädilektionsstellen der EACP betreffen die Extremitäten, die Gluteal-, Inguinal- als auch die Abdominalregion, während Gesicht, Palmae und Plantae stets ausgespart sind, lokalisierte und uniläsionale Formen sind beschrieben [1, 7]. Während die EACP im Erwachsenenalter selten beschrieben ist, wird sie im Kindesalter als häufigste pustulöse Psoriasisvariante genannt [8]. Klassische psoriatische Plaques an den Prädilektionsstellen, eine Gelenkbeteiligung sowie eine positive Familien- oder Eigenanamnese fehlen meist [4]. Die EACP hat einen chronischen, schubweisen Verlauf, medikamentöse und infektiöse Triggerfaktoren sind meist nicht eruierbar [1, 4]. Durch das typische klinische Bild und das Fehlen von Allgemeinsymptomen ist die EACP gut von der Psoriasis pustulosa generalisata abzugrenzen, differenzialdiagnostisch sind subkorneale Pustulose (Sneddon-Wilkinson-Syndrom), Tinea corporis, akute generalisierte exanthematische Pustulose (AGEP) und IgA-Pemphigus (Typ subkorneale pustulöse Dermatose) zu erwägen [4, 9].
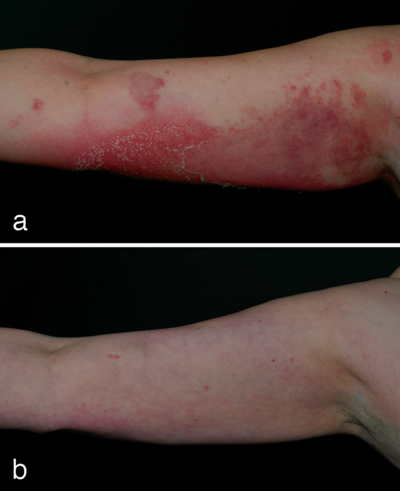
Die Datenlage zur Therapie der pustulösen Psoriasisvarianten ist deutlich schlechter als für die klassische Psoriasis [10]. Systemtherapeutika der ersten Wahl stellen Retinoide dar, gefolgt von Ciclosporin, Methotrexat und Infliximab [10, 11]. Ebenso wird der erfolgreiche Einsatz der Phototherapie genannt, insbesondere die systemische PUVA-Therapie [10]. Auch wenn der Einsatz systemischer Steroide eine rasche Besserung der Symptome bewirken kann, und auch teilweise in den Publikationen Erwähnung findet, sollte diese Therapieoption aufgrund des sicher zu erwartenden Rebound-Phänomens vermieden werden. Die EACP hat quoad vitam eine gute Prognose, die Einschränkung der Lebensqualität ist jedoch nicht unerheblich und äußerst therapieresistente Fälle sind beschrieben [10, 11]. Auch bei dem von uns beschriebenen Fall hatte sich eine Therapieresistenz gegenüber einer Kombinationstherapie mit topischer Applikation von 0,5 % Clobetasolpropionat und Schmalspektrum (311 nm) UV-B-Phototherapie sowie Acitretin (0,5 mg/kg KG), Ciclosporin (2,14 mg/kg KG), Methotrexat (15 mg wöchentlich s.c.) als auch Etanercept (50 mg wöchentlich s.c.) gezeigt. Erst durch den Einsatz einer systemischen Therapie mit Adalimumab (40 mg s.c. alle 2 Wochen) konnte nach vierwöchiger Behandlung eine fast komplette Remission erreicht werden, die sich auch weiterhin nach acht Monaten im Follow-up zeigte (Abbildung 3).
Interessenkonflikt
Keiner.
Literatur
2 Milian G, Katchoura F. Psoriasis pustuleux generalise. Bull Soc Fr Dermatol Syph 1933; 40: 851–2.
3 Lapière S. Recurring psoriasis due to growths of erythemato-squamous elements developing in a few days. Minerva Dermatol 1959; 34: 270–2.
4 Albert A, Hein R, Ring J, Jakob T. Erythema annulare centrifugum-like psoriasis cum pustulatione. Hautarzt 2007; 58: 769–73.
5 Iizuka H, Takahashi H, Ishida-Yamamoto A. Pathophysiology of generalized pustular psoriasis. Arch Dermatol Res 2003; 295 Suppl: S55–9.
6 Keller M, Spanou Z, Schaerli P et al. T cell-regulated neutrophilic inflammation in autoinflammatory diseases. J Immunol 2005; 175: 7678–86.
7 Park YM, Kang H, Cho BK. Annular pustular psoriasis localized to the dorsa of the feet. Acta Derm Venereol 1999; 79: 161–2.
8 Liao PB, Rubinson R, Howard R et al. Annular pustular psoriasis – most common form of pustular psoriasis in children: report of three cases and review of the literature. Pediatr Dermatol 2002; 19: 19–25.
9 Schauer F, Renkl A, Technau-Hafsi K et al. Pruritic intertriginous vesiculopustular eruption. J Dtsch Dermatol Ges 2014; 12: 827–30.
10 Robinson A, Van Voorhees AS, Hsu S et al. Treatment of pustular psoriasis: from the Medical Board of the National Psoriasis Foundation. J Am Acad Dermatol 2012; 67: 279–88.
11 Weishaupt C, Metze D, Luger TA, Ständer S. Treatment of pustular psoriasis with infliximab. J Dtsch Dermatol Ges 2007; 5: 397–9.
<< zurück

Die Diagnosequzze werden uns freundlicherweise zur Verfügung gestellt vom
"Journal der Deutschen Dermatologischen Gesellschaft" © Deutsche Dermatologische Gesellschaft
![Logo: Junge Dermatologen im Berufsverband der deutschen Dermatologen - zur Startseite [ALT+1]](/typo3conf/ext/judermconfig/Resources/Public/Images/Branding/JuDermLogo.png?v=2)