Diagnose
29. August 2017
Kutane Schistosomiasis
Weitere Diagnostik
Weder in Stuhlproben noch im 24 h-Sammelurin ließen sich pathogene Protozoen oder Wurmeier nachweisen. Die Serologie zeigte erhöhte Antikörper-Titer gegen Schistosomen (1 : 64; positiv > 1 : 32); bis auf eine diskrete Eosinophilie von 7 % waren die weiteren Laboruntersuchungen unauffällig. Mikroskopisch ließen sich die Eier bei Vorhandensein eines charakteristischen terminalen Stachels, einer Größe von ca. 150 μm und intraluminalem Nachweis von reichlich Mirazidien als der Spezies Schistosoma haematobium zugehörig klassifizieren. Auf eine weiterführende molekulargenetische Untersuchung zur Erregerdifferenzierung wurde demzufolge verzichtet.
Therapie und Verlauf
Es erfolgte im Abstand von vier Wochen die dreimalige, komplikationslose Verabreichung von Praziquantel (Biltricide®) 40 mg/kg KG oral. Darunter zeigte sich eine deutliche Rückbildung des Knotens am Skrotum. Zudem wurde den Familienangehörigen, welche ebenfalls Afrika bereist hatten, eine Untersuchung hinsichtlich einer Schistosomiasis empfohlen.
Kommentar
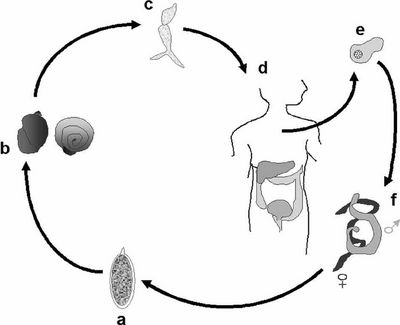
Die Schistosomiasis (veraltet: Bilharziose) ist eine endemische Erkrankung der Tropen und Subtropen mit einer geschätzten Zahl Infizierter von mehr als 200 Millionen Menschen. Der Malawi-See in Ostafrika, in welchem auch unserer Patient während seiner Rundreise gebadet und wo er sich wahrscheinlich auch infiziert hat, ist als Endemiegebiet für die Schistosomiasis gut bekannt [1, 2]. In Afrika sind S. haematobium und S. mansoni die häufigsten Erregertypen, während S. japonicum vorwiegend im asiatischen Raum anzutreffen ist. Die Saugwürmer (Pärchenegel) durchlaufen einen typischen Lebens- und Infektionszyklus (Abbildung 2).
Meist sind viszerale Organe (Dickdarm, Rektum, Harnblase) und deren Gefäßsystem betroffen. Häufig ist die chronische viszerale Infektion asymptomatisch. Jedoch können ernstzunehmende Komplikationen in Form rezidivierender rektaler oder urogenitaler Blutungen im Rahmen einer parasitär bedingten Gefäßarrosion mit resultierender Anämie, abszedierende Entzündungen oder, bei jahrzehntelanger, unbehandelter Bestandsdauer, auch das Auftreten eines Harnblasenkarzinoms sein. Zudem können zu verschiedenen Stadien des Infektionszyklus reaktive, immunmediierte Exantheme („swimmer‘s itch“, „Zerkariendermatitis“), teils verbunden mit Systemzeichen, auftreten [3].
Die Haut ist selten primärer Infektionsort durch direkte Einwanderung von Zerkarien oder – und dies ist weitaus wahrscheinlicher – wird sekundär durch hämatogene Disseminierung der Eier/Würmer mit Embolisation in kutane Gefäße involviert. In der Regel finden sich dann, wie auch bei unserem Patienten, anogenitale Plaques und Knoten [4]. Zu den klinischen Differenzialdiagnosen zählen Zyste, Keloid, Akne inversa oder Fremdkörpergranulom. Extra-anogenitale Lokalisationen wurden bisher äußerst selten beschrieben [5]. Postuliert werden hier eine aktive Migration geschlechtsreifer Würmer durch das klappenlose, paraspinale Venengeflecht oder eine hämatogene Embolisation der Parasiten via portosystemischer Shunts.
Histologisch zeigt sich bei der kutanen Schistosomiasis in Abhängigkeit von der Bestandsdauer der Infektion eine suppurative oder fibrosierende und granulomatöse Entzündungsreaktion mit Nachweis von Wurmeiern oder äußerst selten auch adulten Wurmpaaren auf Weiterschnitten. Die Spezieszuordnung kann aufgrund der Morphologie und Größe der Eier, der Konfiguration eines Stachels an der Wandung der Eier und, sofern notwendig, durch ergänzende molekulargenetische Untersuchungen am Gewebe vorgenommen werden [6].
Praziquantel in einer Dosierung von 40 mg/kg KG ist die Therapie der Wahl sowohl für die viszerale als auch die kutane Schistosomiasis mit sehr guten Heilungsraten [7]. Zu beachten ist, dass Praziquantel nur gegen adulte Würmer wirkt und unreife Parasitenstadien mit dieser Therapie nicht erfasst werden, sodass mit einem Abstand von mehreren Wochen entsprechend dem Entwicklungszyklus der Schistosomen ein bis zwei weitere Sicherheitsbehandlungen zu empfehlen sind. Aufgrund des zunehmenden Fernreisetourismus in tropische Gegenden ist die Schistosomiasis auch für den Dermatologen eine zunehmend wichtige – wenn auch seltene – Differenzialdiagnose bei der Abklärung ungewöhnlicher „Reisesouvenirs“ [8]. Wie in unserem Falle gezeigt, stellt die histologische Untersuchung von klinisch unspezifischen kutanen Indikatorläsionen hierbei einen wegweisenden Schlüssel zur korrekten Diagnosestellung dar, wodurch eine möglicherweise vorliegende ernstzunehmende viszerale Infektion rechtzeitig erkannt und zügig einer adäquaten Therapie zugeführt werden kann.
Danksagung
Wir danken Herrn Dr. Andreas Müller, Institut für Tropenmedizin, Missionsärztliche Klinik, für die weitere therapeutische Betreuung des Patienten.
Interessenkonflikt
Keiner.
Literatur
1 Stauffer JR, Madsen H, Webster B et al. Schistosoma haematobium in Lake Malawi: susceptibility and molecular diversity of the snail hosts Bulinus globosus and B. nyassanus. J Helminthol 2008; 82: 377–82.
2 Madsen H, Bloch P, Makaula P et al. Schistosomiasis in Lake Malawi villages. Ecohealth 2011; 8: 163–76.
3 Soldanova M, Selbach C, Kalbe M et al. Swimmer’s itch: etiology, impact, and risk factors in Europe. Trends Parasitology 2013; 29: 65–74.
4 Reed-Davis L, Theis JH. Cutaneous schistosomiasis: Report of a case and review of the literature. J Am Acad Dermatol 2000; 42: 678–80.
5 Ramdial PK, Calonje E, Singh B et al. Extra-anogenital bilharziasis cutanea tarda revisited. J Cutan Pathol 2009; 36(7): 766–71.
6 Dijk K, Starink MV, Bart A et al. The potential of molecular diagnosis of cutaneous ectopic schistosomiasis. Am J Trop Med Hyg 2010; 83: 958–9.
7 Utzinger J, Keiser J, Shuhua X et al. Combination chemotherapy of schistosomiasis in laboratory studies and clinical trials. Antimicrob Agents Chemother 2003; 47: 1487–95.
8 Logan S, Armstrong M, Moore E et al. Acute schistosomiasis in travelers: 14 years’ experience at the Hospital for Tropical Diseases, London. Am J Trop Med Hyg 2013; 88: 1032–3.
<< zurück

Die Diagnosequzze werden uns freundlicherweise zur Verfügung gestellt vom
"Journal der Deutschen Dermatologischen Gesellschaft" © Deutsche Dermatologische Gesellschaft
![Logo: Junge Dermatologen im Berufsverband der deutschen Dermatologen - zur Startseite [ALT+1]](/typo3conf/ext/judermconfig/Resources/Public/Images/Branding/JuDermLogo.png?v=2)